イランがとうとう泣く子も黙る恐るべき無慈悲極まる報復を開始しました!
イスラエルに向けてシャヘドを含む無人機を 200 機以上飛ばしたとのことです!
これは大変だ!
で、イスラエルと米英は、これの殆どを撃ち落としたとのこと。
「いや~、とうとう報復したぞ!皆の衆!爽快爽快!」ハメネイ談。
そんなことよりも、ヨルダン西岸地区で再び
イスラエル入植者による無法が頻発しているようです。
本来は土地を巡る争いであった紛争ですが、
自らの正当性の根拠として
「ヤハウェの神がこの地は我らのものと約束されておる!
(自分たちが書いた)旧約聖書にそう書かれておる!」
ということになって宗教が絡むように・・・。
「そうかいそうかいそれでは仕方ないよね WWWWWWWWWW」センセ談。
さて、濊貊(わいはく)を祖とするツングース-2 系ですが、
彼らから扶余(ふよ)や沃沮(よくそ)、さらには高句麗が出てきます。
沃沮は単に日本海沿岸部に居住していた同族、ということらしいです。
よくそ~言われます。
が、扶余ともなれば中国文化の影響もあって国家の態を持つようになり、
当時の満州において影響力を持つ一大勢力となりました。
高句麗建国の王は扶余出身ということもあり、
さらには後の百済(くだら)の王は高句麗の末裔と自称しているところから、
百済と近しい関係にあった倭には、
濊貊~扶余~高句麗~百済へと続く
言語を含む何らかの文化的影響力が及んでいる、
と考えるのは合理的だと思います。
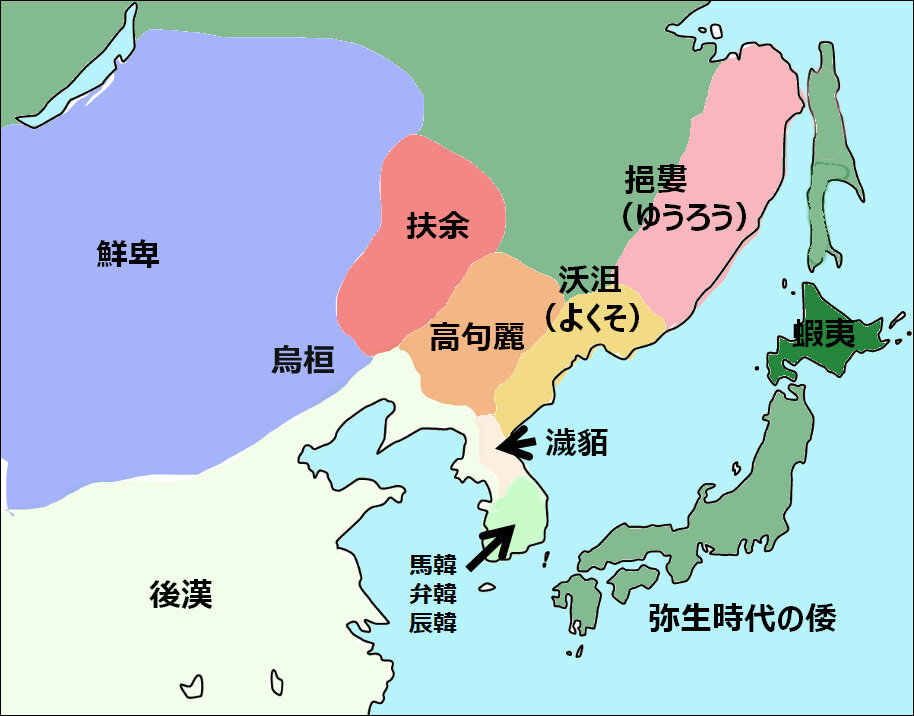 西暦 2 世紀ころの東アジア センセによる
西暦 2 世紀ころの東アジア センセによる
この図からも明らかなように、
ツングース-2 の祖たる濊貊人は強大となった扶余や高句麗に押され、
半島を南下していったようです。
で、この半島南部、韓と呼ばれていた地域には、
水田稲作や海士漁文化を伝えた長江下流域から来た O1b2 の連中や、
「♪ ア~リラン~」とか歌っていたツングース-1 系の連中、
さらには中部は長らく中国王朝の統治下にあったおかげで
漢族系である O2 の連中も多くいたであろうことから、
これらの連中と混交したりケンカしたりで小さな谷ごとに小国が乱立。
長江系が多く居た西南部は馬韓、
ツングース-1 系が多く居た東南部は辰韓、
両者に挟まれた連中は弁韓として、
大雑把なまとまりを見せるようになります。
個人的には、
ツングース-2 系の連中は遼河文明の N の影響も強く受けているのでは?
と思っています。
何しろツングース-1 系よりも内陸部に居住し、
遼河文明にも直接に接していたわけですから。
で、遼河文明の連中はこの地でいち早く農耕を開始していた連中なので、
扶余や高句麗ではコウリャンなどのキビ作が発達し、
さらにはその後の黄河文明の恩恵にも浴して養豚や養蚕も盛んになり、
さすがに水田稲作は無理でしょうが、
より北方のトナカイを飼っていた連中に比べて圧倒的に豊かになり、
鉄器の生産も盛んになりで、
歴史に名を残す王国を築き上げることに成功しました。
歴代中国王朝や同族である高句麗などとはケンカしたり仲直りしたりで
相変わらずの振舞ですが、
そんな扶余も、
西暦 494 年、
ツングース-1 系の勿吉(もっきつ、靺鞨)に滅ぼされてしまいます。
さて、「今月のウクライナ-170」の後半で
過去ログの間違いに関してゴチャゴチャ述べてますが、
ここを読む前に、是非ご一読ください。
読んだら、「今月のウクライナ-170」で引用している過去ログを、
是非ご一読ください。
で、読んだら、ナントかここまで戻ってきて下され。
ハナシはそれからだ!
で、シベリアの少数民族をザザッと見てまいりましたので、
何となくイメージもしやすかろう、と思います。
センセのブログを読んだおかげで
もはや皆様の脳裏にしっかりと焼き付いて夢にまで現れたであろう
「寒冷乾燥の環境に身体的に猛烈に適応した人たち」が、
極東の沿海州から朝鮮半島、満州、モンゴル平原にかけて、
半島を南下する、小国家を作る、大国家を作る、そして最後には
極東~中央アジア~中近東~ヨーロッパにまたがる
史上まれに見る一大帝国を築き上げることとなりました。
もちろん彼ら以前に、
匈奴(フン)、鮮卑、柔然(アヴァール)、突厥、ウイグル、
などがおりましたが、
モンゴルによって全て上書きされ、さらにその後は、
ツングースから身を起こした女真系の大清帝国の時代を迎えることとなります。
で、初めはトナカイを飼っていたりサケ・マスを獲っていたり、
あるいはおしっこで顔を洗っていたりしてた連中ですが、
紀元前 2~3 世紀ころはこういうカンジでした。以下。
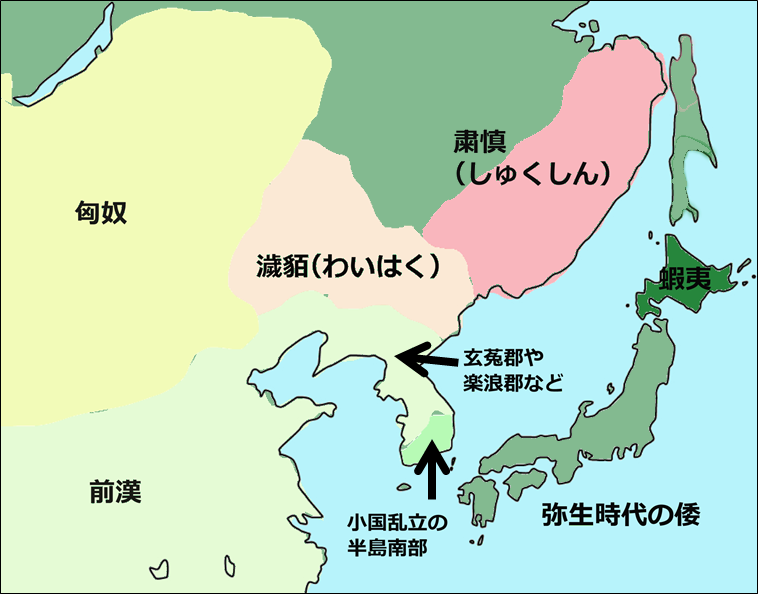 紀元前 2~3 世紀ころの極東地域 センセによる
紀元前 2~3 世紀ころの極東地域 センセによる
濊貊(わいはく)は、正しくは濊と貊に分かれます。
本来は別々の部族だったようですが、兄弟部族みたいな関係だったので、
普通、濊貊と表記されます。
で、彼らが
「今月のウクライナ-170」で訂正されているツングース-2系の先祖です。
「今月のウクライナ-170」で述べている通り、
1系、2系というのはセンセの造語ですので試験では書かないこと!
で、地図で描かれているように、
濊貊はもともと松花江上流域に住んでいたようで、
この地からは彼らの拠点となった濊城も発掘されています。
中国の三国志には濊の記載がありますが、
これによれば、濊の言語~風俗は高句麗とあまり変わらず、
人々の性格~振舞もしっかりしていて、
濊貊の文字から連想されるイメージとは異なり、ナカナカ高評価です。
靺鞨の連中とは大違いです!
で、地図は高句麗登場前のもの。
濊貊から扶余(ふよ)、沃沮(よくそ)、高句麗の流れができますが、
中国の史書によれば、いずれも言葉は似たようなものであったとのこと。
で、恐らくというか間違いないというか、
彼らの遺伝子的情報はないと思いますので確かなことは言えませんが、
C2 主体のツングース系であったと思われます。
で、図の粛慎の連中とは言葉が通じなかったとのことなので、
センセが勝手に濊貊系をツングース-2、
粛慎に連なる連中をツングース-1とした、
ということです。
繰り返しますが、試験には書かないでね!
さて、シベリアの少数民族を一通り概観しましたので、
お次は極東の歴史時代に突入したいのですが、その前に、
これらの少数民族を眺めていていくつか興味深い点があるので
これをちょいと語ってみたいと思います。
ネネツ(サモエード)の写真から明らかなように、
遼河文明を築いた N の連中は典型的なアジア系の顔立ちをしています。
Q のケットの本来の顔立ちがどうなのか、不確定としておきますが、
新大陸に渡った Q は、基本的にアジア系の顔立ちです。
けれども同じインディアンでも、
映画などでおなじみの北米インディアンは基本的アジア系とは結構異なる。
Q + C2 ではああはならない。
過去にヴァイキングの一部が北東部に入植した可能性を考慮に入れても
ああはならないだろう。
となると、基本の Q が新大陸で地域ごとに独自に変化した、
ということになりますが、それはごく自然だと思います。
で、シベリア少数民族の中でも
C2 の低温乾燥環境への適応が非常に印象的です。
この先 C2 の歴史時代の大拡散、特にモンゴルと清王朝のお話になりますが、
この低温乾燥適応の C2 の大拡散前のアジア人の顔立ちとして
「今月のウクライナ-168」で紹介した台湾原住民※を挙げときましたが、
個人的には、ああいう顔立ちがアジア人の基本型かな?と思ってます。
※中国語では先住民=すでに死に絶えた人々、となるので、
この場合は原住民が正しい、とのことです。以上、ウイキより。
センセの祖母、父方も母方も、によく似ています。
YDNA としては O に代表される連中です。
フェゴ島の先住民の顔立ちを見る限り、
たぶん、Q もそうだったと思いますが・・・。
で、C2 の低温乾燥への適応は比較的新しい時代に生じたと思われるので、
C2 の東西南北への大拡散の結果として
現代の我々が知るような、
アジア人の様々な顔立ちのヴァリエーションが生まれた、
と考えられます。
基本は O です。
これに南方ではネグリト系が混交する。
日本では縄文人~アイヌ人が混交する。
C2 的形質には明らかに北 → 南の勾配が見られますので、
この流れは分かりやすい。
台湾原住民は実のところ物凄い連中で、
過去には台湾から大海原に乗り出し、
フィリピン~マレーシア~インドネシア~ミクロネシアは言うまでもなく、
当時は無人の地であったポリネシア全域を我がものとする。
最終的にはマダガスカル、ニュージーランド、イースター島にまで到達し、
多くの野生生物絶滅の原因となる。
ハワイ先住民の顔立ちは台湾原住民のそれと全く同じではありませんが、
これは途中でニューギニアやメラネシアの血を拾ったと同時に、
やはりその地その地で独自に変化したことによるものかと・・・。
で、出アフリカ時の連中は当然ながらアフリカ人だったわけですが、
海岸沿いに東に向かって拡散して南方域に留まった連中は
色々なヴァリエーションはあるものの、
押しなべて南方系の形質を維持している。
C2 の猛烈な寒冷乾燥への適応を考えても、
やはり、人種的形質は気候風土への適応の結果である、
ということがはっきりと理解されます。
同様に、北欧諸人種の脱色化もまた、
日照不足への適応結果であるのは明らかです。
となりますと、
スンダランドから北方に移動し、
長江流域あたりで長い間暮らしていた連中が O の先祖で、
そこら辺の気候風土が「原アジア人」的な顔立ちをもたらした、
と考えられるわけですが、
そうなりますと、
新大陸の Q もまた、基本、原アジア人的特徴を有するのは何故だ?
「今月のウクライナ-100」で紹介したケット人ですが、
mtDNA を見る限りは東南アジアの血が 3 割も混じっている・・・。
となると、やはり Q と R の祖型である P はイラン発ではなく、
他の多くのハプロと同じくスンダランド由来なのか?
仮にそうであるとしたら、
印欧語族もまたスンダランドから来たということになるが、
本当か?!
いや、そうではなく、
イランから北上し、マンモスを追ってシベリアを東進している間に
アジア的形質を獲得した、という可能性も十分ある。
連中、まだトナカイを訓化していなかったので C2 のようにはならず、
原アジア人的にはなったけど、そのまんま新大陸に渡った、
ということか?
などと、頭の中に春霞を抱えたまま
どうでもいいようなことばかり考えているセンセです。
センセのコロナ、長引く・・・。
9 割方大丈夫なのだが、
ちょいと無理すると熱が出てボオ~ッとしてくる・・・。
ふぐを食ってすでに 1 ヶ月以上も経つというのにどういうこっちゃ?
で、体をだましだまし、毎日を生きる今日この頃です。
で、世界情勢ですが、
安定的に、不安定です。
ロシアのコンサートホールでのテロ事件。
せっかくアメリカがプーチンに教えてあげてたのに、あのありさま・・。
一部ではプーチンの自作自演という説もありますし、
何といっても彼には過去があるので可能性は 0% ではありませんが、
色々な情報から判断する限り、
イスラム過激派によるもの、と判断するのが妥当だと思います。
東部戦線はロシアが押し気味。
人海戦術、とまでは言わないけれど、それに近い形で押してます。
いずれ大規模な反攻を計画しているのでしょうけど、
ここまで長引くと、
この秋のアメリカ大統領選挙の結果を待って開始しても OK かと・・・。
ボランティアの救援活動まで攻撃したイスラエル。
バイデンもとうとうぶちぎれた!
で、ネタニヤフ、
検問所の一部を開放するなど、ある程度の軟化を見せたその矢先、
シリアのイラン大使館を攻撃してイラン革命防衛隊の将軍連 7 名が死亡!
イランはすでにこれまで
アメリカ・イスラエル双方からピンポイントで攻撃を受け、
何人もの将官クラスを殺害されてきたが、
全く持って反撃できない。
相当に赤っ恥をかかされているのに何も出来ない・・・。
せいぜいハマスやヒズボラ、フーシなどを焚きつけて線香花火を上げるだけだ。
加えて東部、パキスタンと国境を接するバルチスタン州では
ジャイシュ・アル・アドルという名前の
イスラム過激派のテロにも悩まされている。
1978 年のイスラム革命以降、何か良いことがこの国にあっただろうか?
ビルマの junta が揺れている。
ベネズエラが隣国の一部を併合しようと画策している。
西アフリカでは国家収入の多くを占めるカカオの生産が壊滅的。
来年のバレンタインデーが心配だ・・・。
で、「バレンタインには草加せんべいを送ろう!」
と、早くも埼玉ではキャンペーンが!!!
ホントか?!
どうやらぶり返しで再び頭がボオ~ッとしてきたようだ・・・。
台湾地震で亡くなられた方々にはお悔やみを申し上げます。
ニヴフ=ギリヤーク
 ニブフの親子 ウイキより
ニブフの親子 ウイキより
新光社編「世界地理風俗大系. 別巻〔第3〕」1931年発行
https://dl.ndl.go.jp/info:ndljp/pid/1876894、
https://commons.wikimedia.org/w/index.php?curid=98462998による
親子であるのは大変よく分かります。
遺伝子情報としては、ある調査における YDNA パターンは
C2 が 38.1%、O が 28.6%、P が 19.0%、R1a が 9.5%、その他が 4.8%。
別の調査では、C2 が 71%、O2 が 7.7%、O1a が 3.8%、O1b が 1.9%、
N が 1.9%、Q が 7.7%、D が 5.8%。
二つの調査で結構大きな差がある。
どちらが真相に近いのかは分からない。
R1 はロシア人との混交の結果。
D はアイヌ人との混交の結果。
O2 は中国人との混交の結果。
Q はケット~インディアンの流れ。
P は Q と一緒にここまで来た連中かと・・・。
mtDNA がむしろ特徴的であり、G と Y、特に Y が過半を占める。
以下の図を参照。
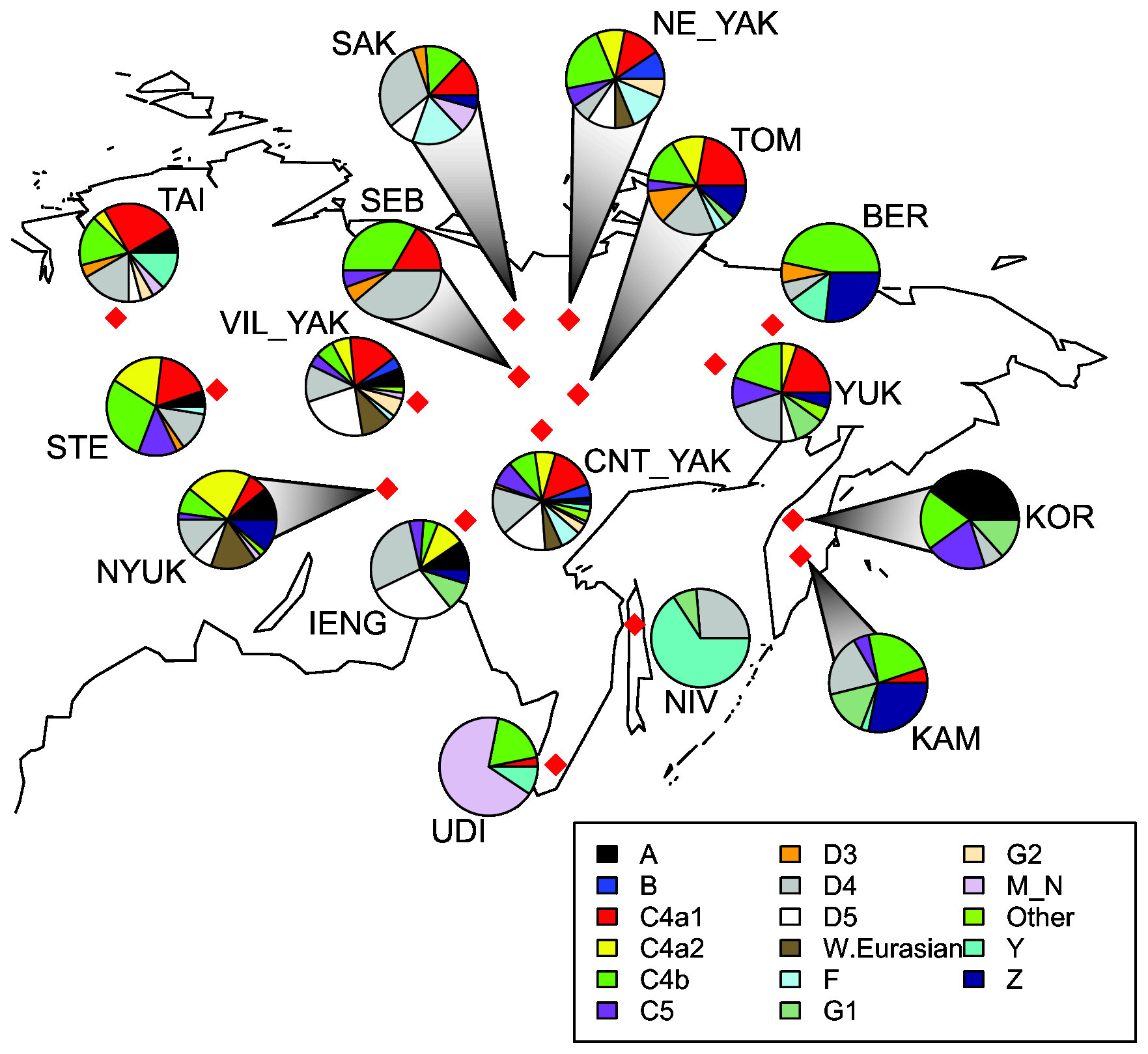 シベリア少数民族の mtDNA ハプロタイプ ウイキより
シベリア少数民族の mtDNA ハプロタイプ ウイキより
https://commons.wikimedia.org/wiki/File:
Map_of_Siberia_-_basic_mtDNA_haplogroup_composition.png
樺太の NIV と示されているのがニブフ。
他のシベリア少数民族のパターンと大いに異なる。
過去ログ「今月の書評-24」で載せたオホーツク人の mtDNA パターンと
よく似てます。
このパターンからも、オホーツク人=ニブフ、と考えられます。
過去ログの mtDNA パターンからは
オホーツク人とアイヌ人との混交も認められます。
ニヴフの言語はウリチやウィルタ(オロッコ)など、
周辺のツングース系諸語とは全く異なり、
むしろ北米インディアンの言語に似ているとの指摘もある。
日本語同様、孤立言語である。
古シベリア諸語(パレオ・アジア語)の一つとして扱われることもあるが、
便宜的であり、仮説の域を出ない。
樺太ニブフの言葉と大陸の黒竜江流域のニブフ語では大きく異なり、
別言語とされることもあるとのこと。以上、ウイキより。
ニブフは、一昔前はギリヤークと呼ばれていた連中です。
YDNA では C2 が優勢ですが、他のタイプも多く混じているようです。
アイヌ人の D が混じるのは地理的~歴史的にも理解されます。
むしろ mtDNA が特徴的で、周辺の連中と大きく異なります。
言語的にも孤立化しており、不思議な民族と言えます。
同じ流れで日本人も相当に不思議なのですが・・・。
以上、センセの偏見による。
ユカギールなどと同じく
北東アジアにおける古参民族の一つと考えられているようで、
ツングース系民族の拡張によって隅に追いやられた、
との説もあるようだ。
アイヌやオロッコ(ウイルタ)など、
他の樺太先住民と共に山丹交易に参加していたようで、
間宮林蔵をベレンまで案内したのはニブフの酋長であった。
 ニブフの夫婦とアイヌのオトコ ウイキより
ニブフの夫婦とアイヌのオトコ ウイキより
https://commons.wikimedia.org/w/index.php?curid=11087602による
手前がニブフの夫婦で後ろで佇んでいるのがアイヌのオトコらしい。
ニブフの旦那の描き様がちょと酷いのではないのか?
いくらなんでも・・・。
奥さんが不憫でならない・・・。
樺太北東岸に住むウイルタがトナカイに執着するのと異なり、
ニブフは漁猟を専らとし、狩猟は副次的で、
トナカイの飼育は殆ど行われない。
サケ・マスの干し肉を主食とするだけでなく、
衣服などもサケ・マスの魚皮で作るとのこと。
 サケ・マスの肉を干すニブフ ウイキより
サケ・マスの肉を干すニブフ ウイキより
https://commons.wikimedia.org/w/index.php?curid=8784864による
自信の伝承によれば、人間は昔は動物であり、
アイヌはクマ、オロッコはトナカイ、そして自分たちは犬であった、
とのこと。以上、ウイキによる。
だもんで、犬を大切にするが、食べたりもする。よくあるハナシ。
アイヌと同じようなクマ祭り(アイヌ語でイヨマンテ)を行うが、
上記伝承を見る限り、アイヌから伝わったのかもしれない。
アイヌのクマ祭り自体が、
東北の縄文人から伝わったイノシシ祭りに由来する、
という説もある。
人口減少に悩んでいた縄文人は多産のイノシシに魅了されていたようだ。
東韃紀行にも書かれているが、
ニブフは女尊男卑の世界であり、
よっぽどのことが無い限り女性は罰せられない、とのことで、
千鶴子センセも大喜び!以上、センセの偏見による。
さて、シベリア少数民族のお話はこれでオシマイ。
興味深い点が多々あります。
北海道~樺太~千島に広がっていたアイヌ人とは
気候風土も似ていることから
共通する文化的要素もたくさんありますが、
人類学的な形質が大いに異なる。
この点が、センセにとっては最も興味深い。
 アイヌのオトコ連 ウイキより
アイヌのオトコ連 ウイキより
不明 - 新光社「日本地理風俗大系 第14巻」より。
https://commons.wikimedia.org/w/index.php?curid=7622713による
当然、遺伝子的にも異なります。
「ニブフの夫婦とアイヌのオトコ」の絵を見ても分かる通り、
C2 由来と縄文系の D 由来とは顔立ちも相当に異なります。
但し、あの旦那さんを C2 の代表とするのはいくらなんでも・・・
とは思いますが・・・。
現代日本人には縄文系の遺伝子が 10% 程度認められますが、
YDNA としてみると、30~40% に数値が跳ね上がります。
地域によって異なりますが・・・。
これが何を意味するのか、卑弥呼にまで遡ってお話したいのですが、
当面は何とかウクライナに到達するのに全力を傾けたいと思います。
で、現代の日本人は、
形質的には両者の混合であることは日常的にも感じられますが、
実は日本人の間では C2 が非常に少ない、
ということも以前に述べたことがあります。
C2 だけでなく、N も少ない・・・。
けれども言語は・・・、というカンジで話を進めていきたいのですが、
次の世紀までお待ちくだされ!
モスクワのテロ事件に大谷クンの通訳問題、
紅麴問題に尊富士の 110 年振りの新入幕優勝と
何かと話題が尽きない今日この頃ですが、
さかき第一研究所と第二研究所が統合されましたので、ご報告いたします。
今後は第一第二の名称はなくなり、
さかき研究所が正式名称となります。
あるいは従来どおり、
喜源テクノさかき研究室が分かりやすいかと・・・。
詳しくは、どうぞ弊社 HP をご覧になってください。
正式には 4 月より統合、という形になりますが、
この週にはほぼほぼ引っ越しも完了し、
実質的にはセンセもすでに今週から詰めています。
高台にありますので、これまでの場所よりも眺望がよく、
北アルプスの峰々もよく見えます。
芝の庭も広いので、
仕事に疲れたらゴルフスイングの練習でも再開するべいと、
良からぬことを企んでいるセンセです。
さて、統合に併せ、
第二研究所で働いていた長山ゆり子さんが先日退職されました。
いわゆる寿退社です。お姉さんのまり子さんに続きます。
いつもながらに
上田の東急 REI ホテル 1F の真田庵でお別れ会を開きました。
 センセからゆりちゃんにお餞別。
センセからゆりちゃんにお餞別。
大ジョッキに盛られた清涼飲料水が目につきますが、
ゆり子ちゃんのタンブラーはすでに 3 杯目です・・・。
なので、お餞別にはホワイトデーのクッキーとは別に、
発酵麦の清涼飲料水券を用意しました。
きっと喜んでいただけるかと・・・。
「自分が貰って嬉しいものをヒトに贈る」、
というのは鉄則ですよね!
 みんなで並んで写真撮影。
みんなで並んで写真撮影。
一人去り二人去りで、研究所も段々寂しくなってまいりました。
でもブログはまだまだ続きますので乞うご期待!
ではゆり子さん、末永くお幸せに!!!
現時点ではブログの表紙、右上の研究所の写真が変更されてませんが、
テクニカルな問題らしいので、そのうち変わるかと思います。
ナナイ
 ナナイの家族 ウイキより
ナナイの家族 ウイキより
https://commons.wikimedia.org/w/index.php?curid=8640786による
中国の影響が強いのが分かります。
遺伝子情報が得られなかったが、C2 主体であるのは明らか。
別称として、ゴルディ、コルドッケなど。
言語はツングース系のナナイ語。
ウィルタ語、ウリチ語とともに南ツングース語派に属す。
1989 年時点において、ロシア国内に約 1 万 2000人弱が住んでいる。
中国にも居住し、2004 年時における人口は 4640 人。
ツングース系の中で、最も南に分布する。
そのため、上の写真でも分かるように、中国文化の影響が強い。
けれども現在では、ロシアの影響がより勝っているようだ。
この先、歴史時代のお話をする予定ですが、
いわゆる靺鞨(まっかつ)はナナイである可能性大。
 ナナイの子供たち ウイキより
ナナイの子供たち ウイキより
https://commons.wikimedia.org/w/index.php?curid=8754993による
左の女の子は寒くて鼻水が垂れている・・・のではなさそうだ!
生業は、河川でのサケ・マス漁などの漁撈が主体で、
トナカイの放牧は行わない。
居住地は魚の豊富な大河や湖の沿岸、河川の河口部。
河川の凍結する冬季には森林での狩猟も行うとのこと。
サケ・マス漁が多いため、昔の衣服はサケ・マスの皮で作った。
基本は魚食であるが、
黒竜江上流部(すなわち南部)のナナイは中国人から穀物栽培を学び、
穀物、野菜、豚肉を多く入手して食生活に役立てた。以上、ウイキより。
「隋書」の靺鞨伝によれば、
靺鞨の先祖がセンセの過去ログで述べた粛慎(しゅくしん)とのこと。
センセの過去ログではオホーツク人=ニブフ(後述)に比定されてるが、
オホーツク人=日本書紀で書かれている「あしはせ」と考えられ、
日本書紀ではあしはせに対して粛慎の文字が充てられているので
この流れだけで考えると粛慎=ニブフ、となりますが、
7 世紀中ごろに活躍した阿倍比羅夫(あべのひらふ)によって討伐される粛慎は
同時代に成立した隋書によれば「靺鞨の先祖」と記載されているので、
時代的に合致しない。
従って、「あしはせ」は本来の粛慎ではない可能性大。
やっぱりオホーツク人はツングース系ではなく、ニブフの可能性が高い、
と思う。
隋書における靺鞨人は「地面に穴を掘って住まう穴居(けっきょ)人で、
尿を用いて顔を洗うなど、周辺諸民族中では最も不潔な連中である!」
と、けちょんけちょんに書かれている。
川沿いに住んでいるのだからもっときれいな水で顔を洗えばよい、
とセンセなんぞは思うが、
たぶん、黒竜江の水は冷たいのでイヤなんでしょうね WWW。
ウイキでは、
「伝統的な住居は、河川の近くに穴を掘り、
白樺樹皮や木材を用いて独特の半円形の家屋をつくって夏季の住まいとし、
冬季には狩猟に適する場所に半地下式の住居を作った」
とのことなので、やはり両者は同族なのであろう。
但し、穴居する部族は靺鞨に限らない。
世界中に、比較的近年まで見られた。
古事記や日本史に出てくる土蜘蛛(つちぐも)も、
たぶん穴居生活を送っていた縄文系の連中だと思います。
宗教は基本的にシャーマニズムであるが、
たぶんモンゴル族などの影響でチベット仏教も浸透したようだ。
ロシアの統治以降はロシア正教への改宗が進んだ。
RUSSIA BEYOND によれば、
1974 年までナナイは名字を持たなかったが、
ソ連政府がパスポート所持を義務化し、名字の必要性が生じたため、
自らの部族名などを名字としたそうだ。
おかげで全名字あわせても 30 個くらいしかない、とのこと。
ウイキのナナイ項によれば、先述したデルス・ウザーラはナナイ人、
と書いてある。
同じウイキのウデヘ項によれば、デルス・ウザーラはウデヘ人、
と書いてある。
ウデヘもナナイも似たもの同士なので、
あまり気にしナナイ方がよい、ということなのであろう。
RUSSIA BEYOND にはナナイの写真が多く載ってます。
ネギダール
部族の写真ナシ!
遺伝子情報も得られなかったが、C2 主体であろう。
ネギダール族の起源は、
エヴェンキを主体としてニヴフ、ナナイ、ウリチとの混血と考えられている。
ツングース系民族の一つで、エヴェンキ語に近いネギダール語を話す。
2002年のロシア国勢調査によると、ロシア国内に567人が暮らし、
そのうち147人がネギダール語を話すとのこと。
主として漁猟で暮らす。以上、ウイキより。
ウデヘ
 ウデヘのオトコたち ウイキより
ウデヘのオトコたち ウイキより
https://commons.wikimedia.org/w/index.php?curid=38291806による
真ん中で偉そうにしているオトコは、
ロシアの探検家、ウラジーミル・アルセーニエフ。
 ウデヘの集落 ウイキより
ウデヘの集落 ウイキより
https://commons.wikimedia.org/w/index.php?curid=38365884による
これも遺伝子情報が得られなかったが、C2 主体であるのは明らか。
同じ文言を繰り返して恐縮です。まだ続くかも・・・。
間宮林蔵が「キャッカラ」と呼んだツングース部族。
森林での狩猟を主とするが、高麗人参の採取~交易も行うようだ。
言葉は南方ツングース諸語に属し、オロチ語と近い。
黒竜江以南のツングースは歴史的には中国の影響が強く、
漢語を話す連中も多いとのこと。
歴史時代になれば
中国文化の影響を大きく受けたツングース国家が現れてくるが、
その後のロシアの拡張により、ロシアの影響も受けるようになる。
1860 年の北京条約によって沿海州がロシアに編入されると、
沿海州のツングース部族は押しなべて
ロシアの影響下に置かれることとなった。
生業は森林での狩猟で、オロチ同様にトナカイの飼育は行わない。
現在ではロシアとの同化が進み、ウデヘ語を話すヒトもわずかとのこと。
以上、ウイキによる。
「今月のウクライナ-17」で紹介したデルス・ウザーラはウデヘ人らしい。
上記リンク先には
ツングース部族の芸術的とも言える写真を多く載せてあるので、
是非、ご参照ください。
リンク先の写真はカラパイアによるものです。
毎年のことながら、坂城ではサクラとハナモモが同時に咲きます。
深い桃色と薄いピンクのコントラストが見事です!
センセも含めて地元のヒトはお花見なんぞは致しませぬ。
この時期の研究所の前の庭。
こんなカンジで、四~五月ころに花々を鉢植えにします。
五月になると、アヤメが咲き始めます。前沢さんが植えました。
街路樹のヤマボウシが咲くころ。
この時期はこんなカンジ。
真夏ともなれば、アサガオが満開に!これも前沢さん由来のもの。
研究所の真夏を飾る花といえばコレ!ノウゼンカズラです!
西暦 2 世紀ころの東アジア センセによる
紀元前 2~3 世紀ころの極東地域 センセによる
ニブフの親子 ウイキより
シベリア少数民族の mtDNA ハプロタイプ ウイキより
ニブフの夫婦とアイヌのオトコ ウイキより
サケ・マスの肉を干すニブフ ウイキより
アイヌのオトコ連 ウイキより
センセからゆりちゃんにお餞別。
みんなで並んで写真撮影。
ナナイの家族 ウイキより
ナナイの子供たち ウイキより
ウデヘのオトコたち ウイキより
ウデヘの集落 ウイキより
黒竜江沿いの C2 の分布図 センセによる
オロチの人々 ウイキより
ウリチの男女 ウイキより
ウリチのオトコ ウイキより